Onicomicosis (Parte 1) ¿Cómo tomar muestras para cultivo?
Las onicomicosis (OM) suelen generar dudas diagnósticas, especialmente con traumatismos ungueales, tumores ungueales o periungueales, psoriasis ungueal, liquen plano ungueal, entre otras entidades (ver próximamente en este blog un post sobre diagnóstico diferecial en onicomicosis). Para su confirmación se recomienda realizar un cultivo con una adecuada toma de muestra.
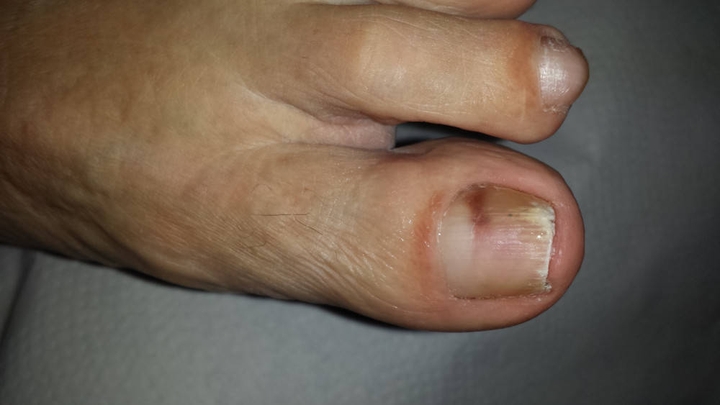
Se presenta el caso de un paciente de 80 años con antecedente de diabetes mellitus (en tratamiento con insulina y metformina) y tinea pedis (TP) en el pie derecho (que no ha tratado de manera regular), que acude a consulta por presentar desde hace dos meses esta distrofia ungueal con cambios en la coloración de la lámina con detritus subungueales (ver figuras 1 y 2), sin dolor ni otra sintomatología.
Se orienta el caso como una probable onicomicosis distal lateral (OMDL), dado el aspecto con diferentes colores, la presencia de detritus subungueales y la tinea pedis concomitante ipsilateral1. Para asegurar el diagnóstico y en previsión de la necesidad futura de tratamiento vía oral se plantea realizar un cultivo de la uña2, 3, según se indica en los siguientes pasos.
Material necesario para la toma de muestras: placas de Petri o recipientes estériles, bisturí, pinzas sin dientes, tijeras/cortauñas estériles y guantes estériles3 (ver figura 3).
A tener en cuenta previamente: no haber realizado tratamiento antifúngico previo (durante los últimos 15 días en caso de cremas, 1 mes en caso de lacas y 1-3 meses en caso de tratamientos sistémicos); cepillar las uñas con agua y jabón 3 veces al día los 3 días previos a la toma de muestra y realizar un baño con sal la noche anterior. Acudir a la consulta con calzado cerrado y medias o calcetines y habiendo retirado el esmalte o laca de todas las uñas.
Método de recogida:
- Colocar una toalla y utilizar guantes estériles, si es posible.
-
Obtener las escamas raspando con un bisturí bajo la lámina ungueal despegada y llegando a la zona dolorosa3 (figuras 4 y 5).
- Cortar con una tijera fina y curva o con cortauñas los fragmentos de la uña afectada. Se ha de obtener el máximo de muestra posible incluyendo zona sana más proximal y detritus de la parte inferior de la placa ungueal. Este paso es básico para proporcionar resultados más fiables.
- En el caso de la onicomicosis blanca superficial se ha de hacer rascando la superficie ungueal.
- Recoger el material obtenido en una placa de Petri o en un recipiente estéril.
- Realizar la solicitud para el laboratorio de microbiología de cultivo de uñas, donde se suele llevar a cabo una observación al microscopio con hidróxido de potasio (KOH) y siembras en agar Sabouraud cloranfenicol y actidiona que se leen semanalmente durante 4 semanas.
Bibliografía y referencias:
- García Hernández D, Ballester Torrens M, Valle Cruells E. Infecciones cutáneas. AMF-Actualización en Medicina de Familia. 2018;14(4):184-197.
- Pereiro Ferreirós M, García-Martínez FJ, Alonso-González J. Actualización en el tratamiento de las micosis cutáneas. Actas Dermosifiliogr. 2012;103(9):778-783.
- Denning DW. Fortnightly Review: Fungal nail disease: a guide to good practice (report of a Working Group of the British Society for Medical Mycology). BMJ. 1995;311:1277.
- Haghani I. Comparison of diagnostic methods in the evaluation of onychomycosis. Mycopathologia. 2013:175:315-21.
- Subías Loren P, Calvet Combelles I. Obtención de material para descartar una micosis. FMC. 2009;16(7):406-8.