VHC: Datos del mundo real sobre la seguridad y la eficacia de los AAD autorizados
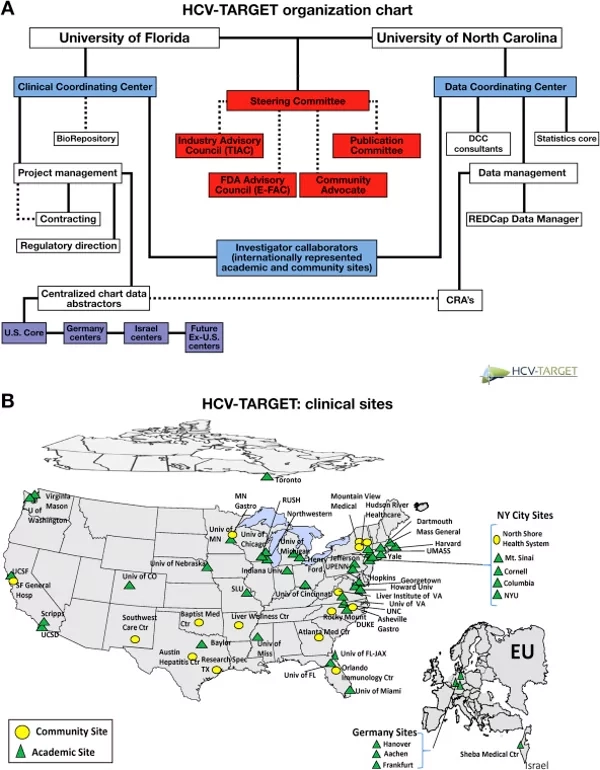
La aparición de los antivirales de acción directa (AAD) ha supuesto un cambio trascendental en las expectativas de curación de los pacientes con infección crónica por el VHC. Son fármacos de elevada eficacia demostrada a nivel de ensayos clínicos y en condiciones clínicas reales (respuesta viral sostenida superior al 90%). Los perfiles de seguridad de estos fármacos se han comprobado a nivel de los ensayos clínicos. Los organismos e instituciones reguladoras Públicas tienen la responsabilidad de salud pública de garantizar la seguridad y la efectividad de los productos farmacéuticos autorizados, como los AAD, en condiciones clínicas reales post-comercialización. En un artículo publicado por Mishra P y colaboradores se describe la creación de una plataforma para recoger datos a nivel mundial y en la práctica clínica real sobre la seguridad y la efectividad de los AAD autorizados para el tratamiento de la infección crónica por VHC. Esta plataforma ha sido propiciada por el Centro de Evaluación e Investigación de Medicamentos (CEDER) de la FDA, División de Productos Antivirales en colaboración con la Red de Registro e Investigación Terapéutica de la Hepatitis C (HCV-TARGET).
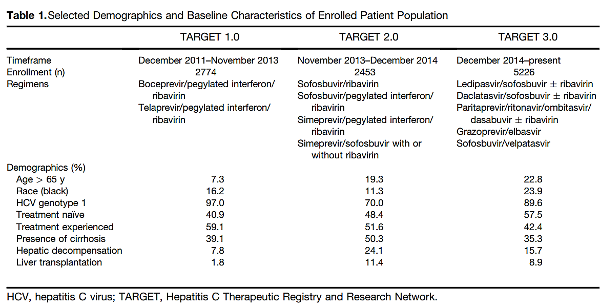
En relación con los resultados, desde su inicio en 2011, HCV-TARGET ha inscripto 10.000 pacientes con hepatitis cróncia por VHC tratados con esquemas basados en AAD.
El protocolo HCV-TARGET permite la inscripción de poblaciones que pueden haber estado subrepresentadas en ensayos clínicos precomercialización (por ejemplo, los pacientes de las minorías insuficientemente representadas), los que tienen cirrosis, la cirrosis descompensada y los que se someten a trasplante de hígado, por ejemplo, han sido sobremuestreados en comparación con la población general de pacientes tratados con hepatitis C.
Los autores reconocen que existen varias limitaciones a la base de datos HCV-TARGET. La más importante es que no hay grupo de control de pacientes no tratados frente a hepatitis C. Sin un grupo de control no expuesto, no siempre se puede determinar la evaluación de la causalidad de los resultados adversos; puede permanecer incertidumbre sobre si las reacciones adversas observadas se deben al régimen de tratamiento, progresión de la enfermedad subyacente, otras condiciones comórbidas y/o efectos secundarios a los medicamentos concomitantes.
Los autores indican que el uso de datos de cohortes observacionales sistemáticamente recopilados, para demostrar la efectividad clínica es prometedor. Los datos sobre la efectividad en el mundo real podrían proporcionar evidencia de apoyo si se incluyen como un componente de una evaluación global del beneficio-riesgo con otros estudios y pueden contribuir a la totalidad de los datos disponibles para la toma de decisiones regulatorias. Los estudios longitudinales de cohorte de seguimiento proporcionan un medio para evaluar los resultados a largo plazo en el establecimiento de la RVS y obtener los datos de seguridad necesarios una vez que se utiliza un fármaco más ampliamente y bajo condiciones más diversas en un entorno real. Los datos generados ayudarán a proporcionar información importante sobre seguridad y efectividad sobre la forma en que los fármacos se realizan en las poblaciones más diversas.
En el futuro se conocerán datos de esta plataforma que permitirán comprobar si se confirman estas posibilidades que se apuntan.