Tratamento da dor crónica: escada do tratamento
A dor crónica é uma doença!
É uma dor que persiste para além do sintoma protetor e potenciador de sobrevivência que é a dor aguda. Surge quando não se soluciona a causa deste sintoma, ou após este adquirir duração ou intensidade suficiente para alimentar fenómenos de sensibilização periférica e central, gerando plasticidade negativa nas vias ascendentes e descendentes da dor. No entanto, mesmo com uma solução corretiva para o evento inicial a dor pode instalar-se e evoluir, exemplo disso são os doentes amputados de um membro inferior que mantém dor no pé amputado, como se ele ainda existisse. Este arrastar do sofrimento gera um ciclo vicioso de ansiedade, medo e stress, envolvendo o doente numa espiral de problemas, que envolvem a família, as emoções e a estabilidade funcional. São causa de forte absentismo laboral, contribuindo para marcados custos financeiros para as famílias, empresas e estado.
A prevalência a nível mundial desta doença é importante, mas ainda assim subdimensionada. Supõe-se que afete 20 % da população mundial, particularmente mulheres e idosos. A maior fatia corresponderá às causas músculo-esqueléticas (30 a 40 %), sendo a patologia oncológica responsável por apenas 1 a 2 %. O segundo lugar do pódio é ocupado pelas cefaleias.
Portanto, fica claro que as medidas para a eliminação/diminuição da dor são essenciais para evitar a sensibilização periférica/central nos processos iniciais. Se o processo já está instalado, o caminho é a potenciação da recuperação da plasticidade negativa através dos mecanismos de modulação alicerçadas nas medidas farmacológicas e não farmacológicas. Mas atenção! A incessante pesquisa clinica da causa e da sua solução nunca devem ser abandonadas.
O médico na elaboração de uma estratégia para o controlo da dor deve dar particular importância a aspetos que serão pilares orientadores para a implementação da mesma. Aspetos como:
- Intensidade da dor.
- Fisiopatologia da dor.
- Patologia associada, idade e risco de polimorfismos genéticos.
- Impacto da dor na funcionalidade e bem estar emocional do doente.
1.Intensidade da dor
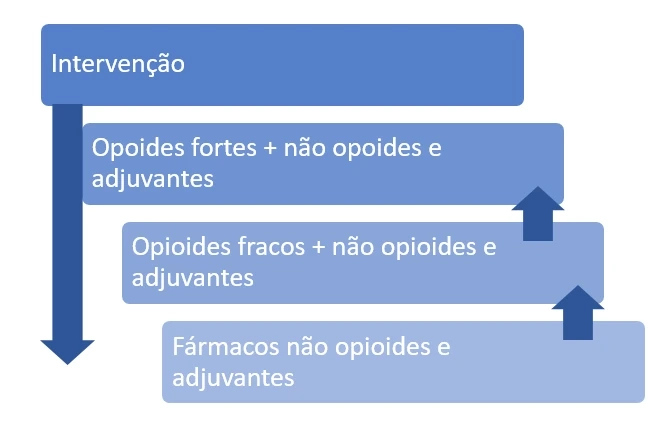
Após a valorização da intensidade da dor através de uma escala como a EVA- Escala Visual Analógica (0 a 10 /ligeira a severa) a decisão pela escolha dos fármacos e a sua gestão devem respeitar a escada da OMS (Figura 1). A estratégia farmacológica na dor ligeira (1º degrau) passa por fármacos não opioides e adjuvantes. A passagem para o 2º degrau (dor moderada ou ligeira que não responda ao 1º degrau) implica a utilização das estratégias do 1º degrau associadas aos opioides fracos. Já o 3º degrau é reservado para a dor severa ou moderada que não tenha respondido ao 2º degrau, através da substituição dos opioides fracos pelos fortes (Figura 2).
Desde alguns anos que a intervenção faz parte do arsenal terapêutico na dor, com provas cientificas dadas e com evidência robusta. A OMS naturalmente passou a incluir as técnicas de intervenção (bloqueios de nervos, infiltrações epidurais, radiofrequência convencional e pulsada, crioablação de nervos, neuroestimulação central e periférica entre outras), como parte da estratégia analgésica na dor. Estas técnicas são assumidas como um 4º degrau, mas não necessariamente a última opção. A sua entrada na escada pode ocorrer a qualquer momento desde que o médico sinta que faz sentido a sua utilização.
2. Fisiopatologia da dor
A identificação da fisiopatologia da dor é mais um dos pilares essências na orientação para o seu tratamento. As estratégias terapêuticas são diferentes de acordo com o tipo de dor: nociceptiva (visceral ou somática) ou neuropática (central ou periférica).
A dor nociceptiva resulta da intensa activação dos neurónios aferentes primários específicos (nociceptores) e deve ser abordada de acordo com a escada analgésica da OMS (FIgura 1), respeitando a progressão multimodal e titulação personalizada.
A dor neuropática tem orientações terapêuticas especificas publicadas em múltiplas guidelines, nomeadamente pela DGS (Direção Geral de Saúde). Após a confirmação dos pré-requisitos para o seu diagnóstico, isto é, 1, existência alterações neurológicas (hipoestesia, hiperalgesia, alodinia) compatíveis com um território nervoso (coerência anatómica) e 2. Teste DN4 positivo (maior ou igual a 4). Se forem cumpridos podemos presumir que estamos perante dor neuropática. A sua abordagem assenta igualmente num esquema em escada divido na seguintes níveis:
Primeira linha
Utilização em monoterapia de antidepressivos ou antipiléticos:
- Amitriptilina, como referencia dos antidepressivos tricíclicos (ADT) ou a nortriptilina ou imipramina como alternativas em caso não tolerância.
- Duloxetina como referência dos inibidores da recaptação da serotonina ou noradrenalina (IRSN) – nos casos de contraindicação aos ADT. Este fármaco é o eleito como de primeira linha para a neuropatia periférica diabética.
- Antipiléticos - gabapentina ou pregabalina.
- Em caso de ineficácia ou intolerância a um deles podemos fazer a rotação entre os dois grupos.
Exceções:
- Nevralgia do trigémio usar a carbamazepina ou oxicarbamazepina se intolerante ao primeiro.
- Idosos acima dos 65 anos (risco de patologia associada e polimedicação), com nevralgia pós-herpética e dor localizada, deve-se usar emplastros de lidocaína a 5 %.
Segunda linha
Se a primeira linha não resultar deve-se optar pela associação dos dois grupos farmacológicos (antipiléticos e antidepressivos).
É ainda 2ª linha :
- No adulto com nevralgia pós-herpética e dor neuropática localizada deve-se associar emplastro de lidocaína a 5 %.
- Adulto com neuropatia localizada, entre as quais neuropatias da diabetes e associadas ao VIH- usar adesivo de capsaicin.
Terceira linha
As medidas farmacológicas a adotar antes do envio para uma Unidade de Dor passam pelo uso de tramadol ou tramadol + paracetamol. Optar pelo tapentadol caso ocorra intolerância ou contra-indicações ao tramadol.
3. Patologia associada, idade e risco de polimorfismos genéticos
A farmacocinética e farmacodinâmica de alguns analgésicos são relativamente complexas devido ao envolvimento das CYP na suas vias de metabolização, alterando a quantidade sanguínea da molécula inicial assim como dos seus metabolitos. O tramadol é um desses fármacos. É um analgésico popular para dores moderadas a fortes, com metabolização a nível hepático pelo citocromo P450, em particular pelas enzimas dos genes CYP2D6 e CYP3A4. A sua metabolização resulta em vários metabolitos, sendo o O-desmetil tramadol, resultante da acção da CYP2D6, o mais ativo. Esta enzima metaboliza um quarto de todas as drogas, incluindo o tramadol. Os humanos podem ser metabolizadores "normais" lentos, intermédios, rápidos ou ultra-rápidos de acordo com as variantes genéticas que apresentam. Infelizmente esse perfil não faz parte da avaliação laboratorial de rotina dos doentes. A FDA refere que os níveis sanguíneos de tramadol são aproximadamente 20 % mais altos, no caso dos metabolizadores lentos quando comparados com os "normais", enquanto os níveis dos metabolitos são inferiores. No caso dos metabolizadores ultra-rápidos as doses do tramadol devem ser reduzidas em 30 %, pela quase certa elevação rápida do metabolito ativo (O-desmetil tramadol) com risco muito aumentado de apneia ou colapso cardíaco. Estima-se que a presença de metabolizadores ultra-rápidos na população caucasiana é de 1 a 3 %, mas como não existe qualquer tipo de rastreio, os clínicos não têm acesso à sua identificação, ficando dependente do surgimento de efeitos secundários severos após a toma deste fármaco. O mesmo ocorre com a codeína, pró fármaco que após metabolização hepática se transforma em morfina. Nos metabolizadores ultra-rápidos a quantidade de morfina na corrente sanguínea pode atingir valores perigosos, com aumentos superiores em mais de 50 % comparativamente com o "normais". A sua utilização deve ser cautelosa e titulada. Outro dos opioides dependentes da CYP2D6 é a oxicodona.
Quanto à patologia associada destacamos a insuficiência renal crónica que condicionará a excreção dos fármacos e seus metabolitos. Os défices de excreção renal condicionam a utilizam de alguns analgésicos. O tramadol, como referido atrás, apresenta um metabolito muito mais potente que o próprio fármaco, e a sua excreção depende do rim. A sua acumulação pode ser perigosa, razão pela qual se aconselha a não utilizar mais do que 100 mg de tramadol/dia em doentes com doença renal no estadio III. O tapentadol pode ter um perfil mais seguro visto que não tem metabolitos ativos, assim como o fentanil. O opioide forte mais seguro nestas circunstâncias é a buprenorfina porque tem uma excreção de 80 a 90 % pelo sistema biliar.
As doses de amitriptilina e os gabapentinoides devem ser reduzidas em doentes com comprometimento na excreção renal, assim como com a venlafaxina (TFG menor que 30 ml/min reduzir para metade a dose diária).
Os doentes com idades mais avançadas são sempre um desafio no tratamento da dor, porque são frequentemente polimedicados (hidromorfona mais segura porque tem baixa ligação às proteínas plasmáticas) e toleram menos os efeitos secundários. Nestes doentes, em particular, é importante a terapêutica multimodal e a titulação gradual de forma a obter adesão e sucesso terapêutico.
4. Impacto da dor na funcionalidade e bem estar emocional do doente
Os quadros complexos da dor crónica são acompanhados de limitações na mobilidade física e na funcionalidade para as atividades diárias; de depressão, de ansiedade e, ainda, de dependência farmacológica. São, por regra, processos arrastados, com soluções parciais, mesmo com correto e empenhado acompanhamento médico.
A identificação precoce de elementos como ansiedade, catastrofismo e depressão como causa ou consequência da cronificação da dor é de extrema importância. A valorização das alterações humorais com implementação de estratégias multidisciplinares farmacológicas e não farmacológicas devem fazer parte da abordagem destes doentes.
O tratamento da dor é habitualmente uma tarefa difícil e complexa, e muitas vezes sem conseguir atingir as expectativas dos doentes. O objetivo em muitos casos não é eliminar completamente a dor, mas sim baixa-la para níveis aos quais o doente se conseguirá adaptar. A avaliação multidisciplinar; a terapêutica personalizada e que menor impacto tiver no dia a dia do doente; a titulação gradual e as abordagens multimodais serão sempre a melhor forma de o fazer.
Bibliografia e referências: